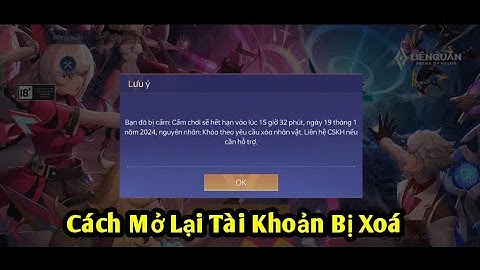
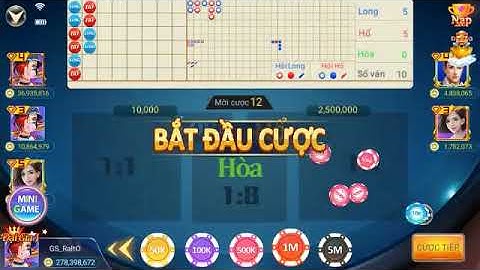
Câu 351932: Trong quá trình bảo quản, một mẫu muối FeSO4.7H2O (có khối lượng m gam) bị oxi hóa bởi oxi không khí tạo thành hỗn hợp X chứa các hợp chất của Fe(II) và Fe(III). Hòa tan toàn bộ X trong dung dịch loãng chứa 0,035 mol H2SO4, thu được 100 ml dung dịch Y. Tiến hành hai thí nghiệm với Y: Thí nghiệm 1: Cho lượng dư dung dịch BaCl2 vào 20 ml dung dịch Y, thu được 2,33 gam kết tủa. Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 20 ml dung dịch Y, thu được dung dịch Z. Nhỏ từ từ dung dịch KMnO4 0,03 M vào Z đến khi phản ứng vừa đủ thì hết 18 ml. Với giải bài 4.9 trang 7 sbt Hóa học lớp 11 được biên soạn lời giải chi tiết sẽ giúp học sinh biết cách làm bài tập môn Hóa 11. Mời các bạn đón xem: Giải SBT Hoá 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li Bài 4.9 trang 7 Sách bài tập Hóa học 11: Hoà tan 1,952 g muối BaCl2.xH2O trong nước. Thêm H2SO4 loãng, dư vào dung dịch thu được. Kết tủa tạo thành được làm khô và cân được 1,864 g. Xác định công thức hoá học của muối. Lời giải: BaCl2.xH2O+H2SO4→BaSO4+2HCl+xH2O1 mol 1 mol1,952M=8.10−3 mol 1,864233=8.10−3 mol Suy ra M = 244g/mol = MBaCl2.xH2O . Từ đó: Suy ra x = 2. Vậy công thức hoá học của muối là: BaCl2.2H2O Xem thêm lời giải sách bài tập Hóa học lớp 11 hay, chi tiết khác: Bài 4.1 trang 6 sbt Hóa 11: Phản ứng nào dưới đây là phản ứng trao đổi ion trong dung dịch?... Bài 4.2 trang 6 sbt Hóa 11: Phản ứng nào trong số các phản ứng dưới đây là phản ứng trao đổi ion trong dung dịch có thể dùng để điều chế HF?... Bài 4.3 trang 6 sbt Hóa 11: Phản ứng tạo thành PbSO4 nào dưới đây không phải là phản ứng trao đổi ion trong dung dịch?... Bài 4.4 trang 7 sbt Hóa 11: Dãy ion nào sau đây có thể cùng có mặt trong dung dịch?... Bài 4.5 trang 7 sbt Hóa 11: Dùng phản ứng trao đổi ion để tách: 1. Cation Mg2+ ra khỏi dung dịch chứa các chất tan Mg(NO3)2 và KNO3... Bài 4.6 trang 7 sbt Hóa 11: HF được sản xuất bằng phản ứng giữa CaF2 và H2SO4. Dùng 6,00 kg CaF2 và H2SO4 đặc, dư thu được 2,86 kg HF... Bài 4.7 trang 7 sbt Hóa 11: Trong y học, dược phẩm Nabica (NaHCO3) là chất được dùng để trung hoà bớt lượng dư axit HCl trong dạ dày... Bài 4.8 trang 7 sbt Hóa 11: Một mẫu nước chứa Pb(NO3)2. Để xác định hàm lượng Pb2+, người ta hoà tan một lượng dư Na2SO4 vào 500 ml nước đó... Bài 4.10 trang 7 sbt Hóa 11: Hòa tan hoàn toàn 0,8 g một kim loại hoá trị II hoà tan hoàn toàn trong 100 ml H2SO4 0,5 M... Bài 4.11 trang 7 sbt Hóa 11: Tính nồng độ mol của dung dịch HCl, nếu 30,0 ml dung dịch này phản ứng vừa đủ với 0,2544 g Na2CO3... Bài 4.12 trang 7 sbt Hóa 11: Trong y học, dược phẩm sữa magie (các tinh thể Mg(OH)2 lơ lửng trong nước), được dùng để trị chứng khó tiêu... Bài 4.13 trang 7 sbt Hóa 11: Hoà tan 0,887 g hỗn hợp NaCl và KCl trong nước. Xử lí dung dịch thu được bằng một lượng dư dung dịch AgNO Siêu phẩm 30 đề thi thử THPT quốc gia 2024 do thầy cô VietJack biên soạn, chỉ từ 100k trên Shopee Mall. Mua ngay
24,4+175,6.10,4100=20,8g Số mol BaCl2: 20,8208=0,1mol Do đó: nH2O=0,1, x mol=24,4−20,818=0,2mol Vậy x = 2. Công thức tinh thể là BaCl2.2H2O.  CÂU HỎI HOT CÙNG CHỦ ĐỀ Câu 1: Phản ứng nào dưới đây là phản ứng oxi hóa khử?
Câu 2: Trong số các chất dưới đây, thuộc loại đơn chất có:
Câu 3: Trong số những chất có công thức hóa học dưới đây, chất nào làm quỳ tím không đổi màu?
Câu 4: Dãy chất nào chỉ bao gồm toàn axit?
Câu 5: Trong số các chất dưới đây, thuộc loại hợp chất có:
Câu 6: Trong số những quá trình và sự việc dưới đây, đâu là hiện tượng vật lí:
Câu 7: Cho biết phát biểu nào dưới đây là đúng?
  |